Estar certificado con esta Norma, es un sello de credibilidad y respaldo para una Empresa que produce bienes o servicios.
ISO genera relaciones mutuamente beneficiosas entre: productores, proveedores y consumidores; incrementa la competitividad, la productividad y facilita la creación de una nueva cultura enfocada al desarrollo sostenible.
Toda organización puede generar confianza mejorar su esquema de trabajo, significa un incremento de sus clientes y gestionar con seguridad el riesgo, reduciendo costos y mejorando la calidad del servicio ofrecido.
La calidad contribuye a todo tipo de organización para tener éxito, a través del incremento de la satisfacción del cliente.
La nueva versión de la Norma ISO 9001:2015 se publicó en septiembre de 2015. Los trabajos para la transición, deben iniciar sin demora.
El cambio más destacado es la incorporación de la gestión del riesgo o un enfoque con base en riesgos.
El plazo para migrar a la versión 2015 es de tres años; quiere decir que toda empresa que se certifica por primera vez a partir del año 2017, tendrá que hacerlo con la nueva versión y las ya certificadas con la versión 2008 deberán migrar durante el año 2017.
Para no poner en riesgo el certificado de calidad es mejor no dejar para último momento; las organizaciones certificadas deben preparar su migración con los tiempos necesarios para solicitar su auditoria.
La nueva versión reestructuró los títulos de los capítulos y el orden de las cláusulas con base en la Estructura de Alto Nivel que se aplicará para las nuevas normas ISO o las versiones futuras.
Estos cambios no afectan el contenido o las exigencias de la Norma ISO 9001, obedece a la conformidad con la composición de las nuevas directrices contempladas en el Anexo SL , para integrar en forma más efectiva todo o parte de varios sistemas de gestión, por ejemplo: parte de la norma de medio ambiente ISO 14001:2015 con la futura norma ISO 45001 (reemplazará la OHSAS 18001:2999) y la ISO 9001:2015, con ello las empresas certificadas alcanzarán cada vez un mayor grado de madurez.
La gestión del riesgo que cada vez se vuelve más fundamental conlleva a su identificación, evaluación y gestión.
La calidad existirá si una organización puede entregar a su cliente un producto o un servicio conforme para el largo plazo; como resultado de una adecuada gestión del riesgo, que se considera superior al contenido estricto del producto o del servicio proporcionado, para alcanzar un perfeccionamiento continuo

La forma de cambio en las organizaciones, exigido por el mercado y las necesidades de los clientes o usuarios, ha llevado a la revisión de la norma para mejorar la práctica del comercio o de la actividad; hoy las empresas de servicio se pueden beneficiar con esta nueva versión por el enfoque de satisfacción del cliente a través del control de riesgo.
A pesar de desaparecer el “Representante de la Dirección”, el compromiso con la calidad mediante un liderazgo fuerte y visible de la Alta Dirección convierten los resultados más participativos para beneficio del cliente, y la política de calidad con sus objetivos serán más coherentes con las estratégicas de dirección.
El “Manual de Calidad” muy arraigado a la cultura de calidad no será exigencia de la nueva versión, habrá que estructurar un documento que consigne en forma ordenada y concreta el sistema de gestión. La exigencia de documentación hace parte de la nueva versión; por tanto, es necesario documentar, mantener y conservar información relevante. Por esa razón un manual de la calidad o como se le quiera llamar seguirá siendo la manera de cumplir con esta exigencia.
La nueva versión le da importancia al contexto que ronda la organización y sus partes interesadas, mediante un análisis e identificación de las partes interesadas con sus expectativas
El conocimiento se convirtió esencial para el desarrollo de cualquier proyecto o negocio. La nueva versión lo contempla como cualquier otro recurso que debe ser gestionado; es necesario identificar el conocimiento necesario para desarrollar la actividad con base en el Sistema de Gestión de la Calidad (QMS) y para alcanzar los objetivos fijados; el conocimiento se mantendrá, protegerá y tenerlo a disposición donde sea necesario.


Los clientes podrán escoger entre las entidades certificadoras SGS, ICONTEC, BUREAU VERITAS, acreditadas en el País por el Ministerio de Desarrollo, la que más les convenga; nosotros los acompañamos hasta la visita de certificación.
- BUREAU VERITAS
- SGS
- ICONTEC
- TUUV RHEINLAND COLOMBIA S.A.S.
- APPUS COLOMBIA LTDA
- ASOCIACION DE EMPRESAS SEGURAS – AES
- CELAC- CENTRO LATINOAMERICANO DE CERTIFICACIÓN S.A.S.SD
- INTERNATIONAL CERTIFICATION & TRAINNING S.A.
- UNIVERSIDAD TECNOLÓGICA DE PEREIRA
- COTECNA
- CIDET
- CONSEJO COLOMBIANO DE SEGURIDAD
- BASC

Certificación a la Gestión de Medio Ambiente ISO 14001:2004
Organizaciones de todo tipo están cada vez más interesadas en alcanzar y demostrar un sólido desempeño ambiental mediante el control de los impactos de sus actividades, productos y servicios sobre el medio ambiente, acorde con su política y objetivos ambientales.
Muchas organizaciones han emprendido “revisiones” o “auditorías ambientales” para evaluar su desempeño ambiental. Sin embargo, esas “revisiones” o “auditorías” por sí mismas pueden no ser suficientes para proporcionar a una organización la seguridad de que su desempeño no solo cumple, sino que continuará cumpliendo los requisitos legales y de su política. Para ser eficaces, necesitan estar desarrolladas dentro de un sistema de gestión que esté integrado en la organización.
Esta Norma Internacional especifica los requisitos para un Sistema de Gestión Ambiental que le permita a la organización desarrollar e implementar una política y unos objetivos que tengan en cuenta los requisitos legalesy la información sobre los aspectos ambientales significativos. Es su intención que sea aplicable a todos los tipos y tamaños de organizaciones y para ajustarse a diversas condiciones geográficas, culturales y sociales


Especificación OHSAS 18001:2.007
La preocupación de las organizaciones por la implementación de sistemas para la gestión eficaz de la seguridad y la salud en el trabajo aumenta día a día. Continuamente se tiene conocimiento de nuevos accidentes, de carácter grave o incluso mortales, que han tenido lugar en el trabajo.
Toda práctica laboral, comporta determinados riesgos, de mayor o menor nivel, y todas las partes implicadas tienen el deber de lograr que ésta se realice sin perjuicio de la seguridad y la salud del trabajador. El tema de la seguridad y la salud laboral afecta a todas las organizaciones, independientemente de su tamaño y sector al que pertenezcan, hasta tal punto, que éstas, por fin se están decidiendo a tomar medidas importantes, tanto para fomentar la seguridad en sus estructuras organizacionales e instalaciones, como para cumplir con las obligaciones legales aplicables en estas materias.
En la actualidad, la prevención de riesgos laborales se ha convertido en un factor más a tener en cuenta en la gestión diaria de las empresas, por ello están fomentando una actitud proactiva y responsable hacia la seguridad en todos los niveles, impulsan una amplia participación del personal en las tareas preventivas, así como una importante dedicación de tiempo y esfuerzo para mantener la organización viva y productiva en el análisis de los riesgos, la adopción de medidas preventivas y correctivas, la aportación de ideas para la mejora de la seguridad de sus instalaciones y la promoción de comportamientos seguros en todo el personal, todo ello dentro de un proceso de mejora continua.


ISO 15189:2012
ISO 15189 fue elaborada por el Comité Técnico ISO/TC 212 (Clinical Laboratory Testing and In Vitro Diagnostic Systems) tomando como referencia las normas ISO / IEC 17025 e ISO 9001.Esta Norma contempla los requerimientos que cualquier laboratorio clínico que analiza muestras biológicas de origen humano, debe cumplir para sustentar que:
- Disponen de un sistema de gestión de la calidad.
- Es técnicamente competente.
- Es capaz de producir resultados técnicamente válidos.
Adicionalmente comprende dos anexos, las recomendaciones para la protección de los sistemas de información del laboratorio y la ética en el laboratorio clínico.
Con el cumplimiento de esta Norma de puede demostrar, garantía sobre el funcionamiento del laboratorio (control de procesos, satisfacción de requisitos técnicos) y generar la información necesaria para el diagnóstico clínico. Existe un compromiso internacional para crear sistemas de detección y respuesta a los problemas de salud pública, uniéndose al proceso de implementación del Reglamento Sanitario Internacional.
Se pretende generar resultados analíticos en los que la comunidad internacional pueda confiar en casos de emergencia.
REQUISITOS PARA IMPLEMENTAR ISO 15189
- Personal competente y calificado.
- Pensamiento con base en el riesgo, como un elemento dinamizador del enfoque a procesos.
- Comunicación de valores críticos para asegurar la seguridad del paciente.
- Adecuada gestión y notificación de información sensible para los pacientes.
- Equipos de laboratorio, reactivos y material fungible, insumos críticos para la realización del trabajo diario en un laboratorio
- Gestión para la optimización de procesos y obtención de la máxima calidad en el servicio ofrecido.
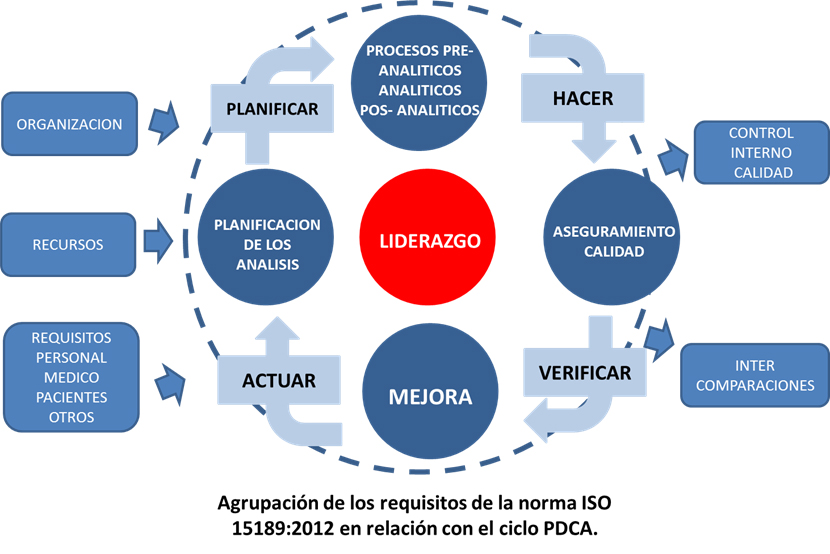
- Control sobre los procesos clave de un laboratorio clínico: procesos pre-analíticos, analíticos y pos-analíticos.

DESARROLLO
- Mantener actualizado un programa de inducción del personal, que tenga en cuenta: calendario laboral, horarios, tipo de vestuario/uniforme de trabajo, instalaciones, requisitos de salud laboral, instrucciones de emergencia y los servicios de salud ocupacional.
- Generar formación a los profesionales en el sistema de gestión de la calidad, los procesos/procedimientos asignados, el sistema de información aplicable, la salud y seguridad, la ética y la confidencialidad del paciente.
- Proporcionar al personal acceso adecuado a los sanitarios, a un suministro de agua apta para el consumo y a las instalaciones para el almacenamiento del equipo de protección personal y ropa de trabajo.
- Hacer el seguimiento, control y registro de las condiciones ambientales, que puedan influir sobre la calidad de la muestra, los resultados y/o la salud del personal, como: iluminación, esterilidad, existencia de polvo, humos nocivos o peligrosos, interferencia electromagnética, radiación, fuentes de alimentación eléctrica, temperatura, niveles acústicos y de vibración.
- Implantar un programa de mantenimiento de los equipos utilizados para realizar las pruebas solicitadas, donde se sigan como mínimo las instrucciones del fabricante.
- Verificar el sistema eléctrico de los equipos, los dispositivos de emergencia, y eliminación de residuos generados por el equipo.
- Controlar un inventario de los reactivos y material fungible; de los lotes de los reactivos y materiales (incluidos los materiales de control y calibración), así como su fecha de recepción, fecha de caducidad, número disponible, etc.
- Mantener actualizados los documentos que describan la organización del proceso pre-analítico, mediante un listado de todos los centros/servicios de procedencia de las muestras, con el nombre del responsable y/o coordinador de cada centro.
- Respecto a la validación de los métodos, realizar la verificación de los mismos y contener como mínimo, cálculo de la precisión y veracidad de los niveles de decisión clínica.
- Mantener ensayos de comparativos con otros laboratorios.
EXIGENCIA
En la actualidad, la acreditación de los laboratorios clínicos según La Norma ISO 15189, se convierte rápidamente en la norma mundial de excelencia para los laboratorios clínicos.Los laboratorios que ostentan la acreditación en ISO 15189 disfrutan de un reconocido prestigio en su sector. Estamos en capacidad de acompañar al laboratorio, en la realización de una autoevaluación objetiva del correcto funcionamiento del proceso global y avanzar hacia la excelencia del servicio ofrecido.
- Identificar sus procesos (pre-analíticos, analíticos y pos-analíticos), e implementar indicadores eficaces para evaluar el desempeño de los mismos.
- Implementar un sistema de gestión con base en procesos adaptados a su organización, y de fácil comprensión para todo el personal.
- Gestionar de forma adecuada sus riesgos y ayudar a asegurar la seguridad del paciente. en las fases pos-analíticas, es donde suceden el mayor número de errores y más concretamente en la pre-analítica.
- Facilitar la labor del médico aportándole una confianza añadida en la fiabilidad del resultado que obtiene.
- Facilitar la aplicación y el mantenimiento de un sistema efectivo de la calidad, dar confianza al usuario en la utilización del servicio.
- Evaluar a sus proveedores, una de las partes interesadas más relevantes de cualquier laboratorio, y cuya falta de control o mal servicio origina pérdidas económicas muy importantes, y disminución de la calidad del servicio ofrecido.

SISTEMAS DE GESTIÓN DE LA CALIDAD PARA INSTITUCIONES DE FORMACIÓN PARA EL TRABAJO
El sistema de gestión de la calidad está influenciado por los diferentes objetivos de la formación para el trabajo, por las definiciones del proyecto educativo institucional (PEI) o su equivalente, por la lectura permanente del contexto socioeconómico en que se encuentra inmerso, por la participación de la comunidad educativa y por prácticas administrativas y financieras específicas en cada institución. Por consiguiente, puede esperarse que los sistemas de gestión de la calidad varíen de una institución a otra.
Para certificarse en las Normas Técnicas de Formación para el Trabajo, hay requisitos que deben tener en cuenta las instituciones de formación para la implementación de un sistema de gestión de la calidad que armonice con los proyectos educativos institucionales, la práctica educativa y los requerimientos del entorno productivo, económico y social.
Las Normas Técnicas de Formación para el Trabajo, establecen los requisitos del sistema de gestión de la calidad para instituciones que forman profesionales o técnicos para el trabajo, acorde con la legislación vigente, enfocadas a las instituciones de educación media técnica, las instituciones de educación para el trabajo y el desarrollo humano, las instituciones de educación superior que ofrezcan programas del nivel técnico profesional y tecnológico de formación para el trabajo, las empresas que desarrollen procesos de formación organizados y sistemáticos para sus trabajadores actuales o potenciales, que ofrecen programas de formación para el trabajo y las cajas de compensación familiar que presten servicios de formación para el trabajo.
Una Institución de Formación para el Trabajo debe certificarse con la norma técnica que corresponda a su sistema de gestión, para:- demostrar la capacidad para proporcionar de forma coherente servicios de formación para el trabajo que satisfagan los requisitos de sus clientes, estudiantes y el entorno productivo, económico y social, y la normatividad vigente
- aumentar la satisfacción de sus clientes, estudiantes y el sector productivo a través de la aplicación eficaz del sistema, incluidos los procesos para la mejora continua del mismo y el aseguramiento de la conformidad con los requisitos del cliente y los reglamentarios aplicables.
Todos los requisitos de las norma técnicas que contengan programas de formación para el trabajo son genéricos y se pretende que sean aplicables a todas las instituciones que ofrecen servicios de formación para el trabajo sin importar su tipo, tamaño y programas ofrecidos, siempre y cuando éstos a apunten a desarrollar competencias laborales, específicas o transversales, asociadas con la Clasificación Nacional de Ocupaciones-CNO, las cuales habilitan a las personas para ejercer una actividad productiva, en un empleo o en un emprendimiento por cuenta propia.
Las instituciones de formación para el trabajo son las siguientes:- Instituciones de educación para el trabajo y el desarrollo humano
- Instituciones de educación media técnica
- Instituciones con programas técnicos profesionales y tecnológicos de educación superior que cuenten con registro calificado otorgado por el Ministerio de Educación Nacional y que sean de formación para el trabajo
- Cajas de compensación familiar que ofrecen servicios de formación para el trabajo
- Las empresas que desarrollen procesos de formación organizados y sistemáticos para sus trabajadores actuales o potenciales, que ofrecen programas de formación para el trabajo
Referencias Normativas
NTC 5555; Sistemas de Gestión de la Calidad para instituciones de formación para el trabajo.
NTC 5581; Programas de Formación para el Trabajo.

Certificación en Inocuidad alimentaria – ISO 22000
La norma ISO22000, está relacionada directamente con la inocuidad de los alimentos en toda la cadena alimentaria y la optimización de los procesos debido a que gestiona la calidad y seguridad de estos.
Genera al interior y exterior de la empresa confianza tanto en la seguridad higiénico- sanitaria como en la calidad de los productos, para aumentar la competitividad en el mercado. Como todos los estándares internacionales ISO, busca un fin, desarrollar un producto de calidad con el mejor servicio posible generando la mejora continua en los procesos del sistema de gestión.
El sistema de gestión de inocuidad de alimentos está sustentado en varios factores:
- Apoyo por la dirección
- Referencia a la normativa aplicable
- Controles de procesos
- Sistema HACCP/APPCC
- Planes de mejora
Implementación, Mantenimiento y Mejora
Existen unas etapas para el proceso de implementación que se tendrá en cuenta a modo orientativo, siendo necesaria personalizarlas para cada organización donde se vaya a implantar el sistema de gestión de inocuidad de los alimentos, basado en la norma ISO22000.
En cada una de las etapas se hará mención de los documentos necesarios para su desarrollo, implantación, mantenimiento y mejora, cumpliendo con los requisitos de la norma ISO 22000, legales y las necesidades de la empresa.
- Conformación del equipo de inocuidad
- Definición del organigrama y responsabilidades
- Determinación de la política de inocuidad
- Determinación de los objetivos
- Planificación del sistema de gestión
- Comunicación de la implementación
Para iniciar el proceso de implementación se debe establecer inicialmente el compromiso de la alta dirección con el sistema, de tal manera que el sistema funcione de forma correcta.
Así mismo se deben establecer las funciones y responsabilidades de la alta dirección.
Posteriormente se debe realizar un diagnóstico inicial de la organización lo que servirá como base para definir la política de inocuidad de los alimentos, las actividades a llevar a cabo y los pasos necesarios para implantar el sistema de gestión de la inocuidad de los alimentos.
Es importante tener en cuenta los siguientes aspectos en relación al diagnóstico inicial:
- Organigrama de la organización.
- Actividad de la organización.
- Sistema de gestión implementado (si los tiene).
- Procesos y productos que elabora.
- Certificaciones y acreditaciones (si los tiene).
- Clientes y proveedores.
- Recursos disponibles (humanos, tecnológicos, materiales etc.).
Cuando la alta dirección determine la conveniencia de iniciar el proceso de implementación del sistema, debe designar un responsable el que tendrá dentro de sus funciones la de llevar el peso de la parte técnica y organizativa del proceso de implantación, es decir se debe conformar el comité de inocuidad de los alimentos; desinando el líder.
El líder del comité de inocuidad tendrá dentro de otras funciones las siguientes:
- Dirigir y coordinar el trabajo del comité.
- Cumplir con los tiempos de implantación del sistema de gestión.
- Servir de enlace entre el equipo y la dirección.
La alta dirección debe designar la jerarquía, funciones y responsabilidades de los integrantes del sistema de gestión y darla a conocer a todos los trabajadores de la organización.
El primer paso es documentar la política de inocuidad de los alimentos la que debe estar definida, documentada y comunicada al resto de la organización. La política debe estar acompañada de los objetivos de inocuidad; los que deben ser medibles con el fin de poder comprobar si el sistema está funcionando de forma correcta.
Una vez definida la política, se debe establecer la planificación del sistema con el fin de definir e identificar los peligros potenciales, comunicarlos y evaluar periódicamente el sistema de gestión.
El responsable del sistema posteriormente debe elaborar un plan de trabajo para poder determinar los tiempos y actividades a desarrollar, este plan puede contener entre otros:
- Documentación a diseñar
- Responsables de los documentos
- Tiempos para cumplir las actividades
- Programación de formación
Igualmente se debe elaborar el presupuesto donde se establecen los recursos necesarios para la elaboración, implementación, mantenimiento y actualización del sistema de gestión de la inocuidad. Se debe incluir el estudio de las infraestructuras y posibles carencias de la organización a la hora de cumplir con la política y los requisitos de la Norma ISO22000.
Todo lo que se ha descrito hasta el momento debe ser comunicado por el equipo de inocuidad a todos los integrantes dela organización ya sea de forma individual o colectivo.
Fase Documental del sistema de Gestión de Inocuidad
Determinar los puntos/procedimientos/fases operacionales que pueden controlarse para eliminar riesgos o reducir al mínimo la probabilidad de que se produzcan (puntos críticos de control (PCC)). Se entiende por «fase» cualquier etapa de la producción y/o fabricación de alimentos, incluidas la recepción y/o producción de materias primas, su recolección, transporte, formulación, elaboración, almacenamiento, etc.
Esta fase está determinada por las siguientes etapas:
- Determinación Programa Prerrequisitos
- Fichas técnicas Producto Terminado y Materia Prima
- Elaboración de diagrama de flujo
- Identificación y evaluación de peligros
- Selección de medidas preventivas
- Establecimiento del plan HACCP/APPCC (Análisis de Peligros y Puntos Críticos de Control)
- Actualización de la información
- Control y manejo de producto no conforme
- Procedimiento de validación
- Procedimiento de verificación
- Procedimiento de actualización
Posteriormente se deben establecer las actividades relacionadas con la seguridad alimentaria es decir, la planificación, y realización de productos inocuos. Se inicia por los programas prerrequisitos y los prerrequisitos operativos, para ello se debe tener en cuenta todas las posibles fuentes y vías de contaminación tales como (instalaciones, materia prima, insumos, equipos, manipuladores); Estos PPR (programas prerrequisitos) deberán estar documentados y tener los registros correspondientes, como pueden ser los de las medidas de seguimiento, las actividades de verificación, las actualizaciones, etc.
Los PPR (programas prerrequisitos), dependen de las características de la empresa, sin embargo se pueden considerar los siguientes:
- Limpieza y desinfección
- Control de plagas.
- Control de residuos.
- Suministro y tratamiento de agua.
- Mantenimiento preventivo de equipos, instalaciones y maquinaria.
- Buenas prácticas de manufacturas.
- Formación.
- Proveedores.
- Trazabilidad (se puede incluir como requisito o se pude determinar de forma independiente).
Una vez establecidos los programas prerrequisitos (PRR), el equipo de inocuidad debe elaborar los siguientes documentos:
- Fichas técnicas de las materias primas
- Fichas de producto final
SI ES DE SU INTERES PUEDE COMUNICARSE CON NOSOTROS PARA ANLIZAR SU NECESIDAD Y GENERARLE UNA SOLUCION QUE SE CONVIERTA EN OPORTUNIDAD DE NEGOCIO. Contáctenos

En el marco de lo dispuesto por el artículo 14 del Decreto 2200 de 2005, modificado por el artículo 4° del Decreto 2330 de 2006, mediante Resolución 1403 de 2007, se determinó el Modelo de Gestión del Servicio Farmacéutico, se adoptó el Manual de Condiciones Esenciales y Procedimientos del Servicio Farmacéutico y se dictaron otras disposiciones.
El parágrafo del artículo 8° de la Resolución 1403 de 2007 (Modelo de Gestión del Servicio Farmacéutico) estableció que la mención que se hace en distintas normas nacionales sobre Buenas Prácticas de Manufactura, en relación con los procesos del servicio farmacéutico reglamentados en la Resolución 1403 de 2007 y el manual que adopta, se entenderá referida a las Buenas Prácticas de Elaboración.
La Certificación de Buenas Prácticas de Elaboración se aplica a los Establecimientos Farmacéuticos señalados en el parágrafo 5° del artículo 11 del Decreto 2200 de 2005 y Servicios Farmacéuticos de Instituciones Prestadoras de Servicios de Salud, que elaboren preparaciones magistrales y que realicen las operaciones de elaboración, transformación, preparaciones, mezclas, adecuación y ajuste de concentraciones de dosis, reenvase y reempaque de medicamentos, dentro del Sistema de Distribución de Medicamentos en Dosis Unitaria para pacientes hospitalizados y/o ambulatorios en casos especiales.
Las preparaciones magistrales que pueden elaborar en el territorio nacional (Colombia), los establecimientos farmacéuticos y servicios farmacéuticos mencionados anteriormente corresponden a: mezclas de nutrición parenteral; mezclas y/o adecuación y ajuste de concentraciones de medicamentos oncológicos y demás medicamentos para cumplir con las dosis prescritas; y preparaciones extemporáneas.
En tal virtud, en Colombia, le corresponde al Ministerio de la Protección Social adoptar el Instrumento de Verificación de Cumplimiento de Buenas Prácticas de Elaboración para los Establecimientos Farmacéuticos señalados en el parágrafo 5° del artículo 11 del Decreto 2200 de 2005 y Servicios Farmacéuticos de Instituciones Prestadoras de Servicios de Salud, que elaboren preparaciones magistrales y que realicen las operaciones antes señaladas.
Como conclusión, el Ministerio de la Protección Social generó la Resolución 0444 de 2007, de obligatorio cumplimiento

Adopción.
Adoptar, para ser aplicado en todo el territorio nacional y con carácter obligatorio, el Instrumento de Verificación de Cumplimiento de Buenas Prácticas de Elaboración para los Establecimientos Farmacéuticos señalados en el parágrafo 5° del artículo 11 del Decreto 2200 de 2005 y Servicios Farmacéuticos de Instituciones Prestadoras de Servicios de Salud, que elaboren preparaciones magistrales y realicen las operaciones de elaboración, transformación, preparaciones, mezclas, adecuación y ajuste de concentraciones de dosis, y reenvase y reempaque de medicamentos dentro del Sistema de Distribución de Medicamentos en Dosis Unitaria para pacientes hospitalizados y/o ambulatorios en casos especiales.
Procedimiento para la obtención del certificado de cumplimiento de las buenas prácticas de elaboración.El procedimiento para la obtención del Certificado de Cumplimiento de las Buenas Prácticas de Elaboración, se adelantará conforme a lo señalado en el Decreto 549 de 2001, o la norma que lo modifique, adicione o sustituya. Igualmente, el interesado en la solicitud de la visita, previa a la obtención del Certificado de Cumplimiento de Buenas Prácticas de Elaboración, deberá allegar debidamente diligenciado el Instrumento de Verificación que se adopta con la presente resolución.
Vigencia del certificado.El Certificado de Cumplimiento de Buenas Prácticas de Elaboración tendrá una vigencia de cinco (5) años, contada a partir de la fecha de su expedición. Dicho certificado podrá renovarse por un período igual, para lo cual, se deberá surtir el procedimiento previsto en el artículo 2° de la presente resolución.
Visitas de inspección.El Instituto Nacional de Vigilancia de Medicamentos y Alimentos- INVIMA, realizará por lo menos una vez al año, una visita de inspección a los Establecimientos Farmacéuticos y Servicios Farmacéuticos de Instituciones Prestadoras de Servicios de Salud de que trata la presente resolución, que elaboren preparaciones magistrales y que realicen las operaciones de elaboración, transformación, preparaciones, mezclas, adecuación y ajuste de concentraciones de dosis, y reenvase y reempaque de medicamentos dentro del Sistema de Distribución de Medicamentos en Dosis Unitaria para pacientes hospitalizados y/o ambulatorios en casos especiales, con el fin de verificar el cumplimiento de las Buenas Prácticas de Elaboración que a la fecha de la visita se encuentren vigentes. Adicionalmente, podrán realizar la(s) visitas(s) que considere(n) conveniente(s), cuando las circunstancias lo ameriten.
Sanciones.Si en ejercicio de las facultades de inspección, vigilancia y control, el Instituto Nacional de Vigilancia de Medicamentos y Alimentos – INVIMA o la autoridad competente comprueba que el Establecimiento Farmacéutico o el Servicio Farmacéutico de Instituciones Prestadoras de Servicios de Salud que realicen las operaciones de elaboración, transformación, preparaciones, mezclas, adecuación y ajuste de concentraciones de dosis, y reenvase y reempaque de medicamentos dentro del Sistema de Distribución de Medicamentos en Dosis Unitaria para pacientes hospitalizados y/o ambulatorios en casos especiales, y/o que elaboren preparaciones magistrales de que trata la presente resolución, no cumple con las condiciones que sustentaron la expedición del Certificado de Cumplimiento de Buenas Prácticas de Elaboración, procederá a aplicar las medidas de seguridad o sanciones, de conformidad con lo establecido en la Ley 09 de 1979, sin perjuicio de las otras sanciones a que haya lugar, y a la cancelación de la certificación respectiva mediante acto administrativo debidamente motivado.
Para certificarse con el INVIMA en Buenas Prácticas de Elaboración, se debe tener en cuenta:
Factores locativos: corresponde a las áreas y/o espacios donde funcionará el Servicio Farmacéutico; en primer lugar debe ser aislado y libre de sectores con contaminación; ventilado, iluminado y bien aireado con condiciones climáticas y de humedad controladas; perfectamente delimitadas.
Procesos internos: comprenden desde la recepción técnica hasta la dispensación, pasando por el reenvase y reempaque que conforman la distribución en Dosis Unitarias.
Competencias del personal: El Decreto 2200 de 2005, en su Artículo 11. Establecimientos farmacéuticos. Afirma, “se consideran establecimientos farmacéuticos mayoristas: los Laboratorios Farmacéuticos, las Agencias de Especialidades Farmacéuticas y Depósitos de Drogas, y establecimientos farmacéuticos minoristas: Las Farmacias-Droguerías y las Droguerías”.

Los establecimientos farmacéuticos solo están obligados a cumplir con las disposiciones contenidas en el decreto 2200 de 2005; en la Resolución 1403 de 2007 (modelo de gestión del servicio farmacéutico) y demás normas que los modifiquen, en relación con los medicamentos y dispositivos médicos.
1.Farmacias Droguerías: La dirección estará a cargo exclusivamente del Químico Farmacéutico. Estos establecimientos se someterán a los procesos de:
a) Recepción y almacenamiento.b) Dispensación.
c) Preparaciones magistrales.
2. Droguerías: La dirección estará a cargo del Químico Farmacéutico, Tecnólogo en Regencia de Farmacia, Director de Droguería, Farmacéutico Licenciado, o el Expendedor de Drogas. Estos establecimientos se someterán a los procesos de:
a) Recepción y almacenamiento.b) Dispensación.
3. Agencias de Especialidades Farmacéuticas: La dirección estará a cargo del Químico Farmacéutico o del Tecnólogo en Regencia de Farmacia. Estos establecimientos se someterán al proceso de recepción y almacenamiento.
4. Depósitos de drogas:
Depósitos de drogas donde se realice el proceso especial de reenvase. La dirección estará a cargo exclusivamente del Químico Farmacéutico. Estos establecimientos se someterán a los procesos de:a) Recepción y almacenamiento.
b) Reenvase.
c) Depósitos de drogas donde no se realice el proceso especial de reenvase. La dirección estará a cargo del Químico Farmacéutico o del Tecnólogo en Regencia de Farmacia. Estos establecimientos se someterán al proceso de recepción y almacenamiento.
Los establecimientos farmacéuticos y personas autorizadas quedan sometidos a los requisitos y técnicas establecidos por las normas especiales y el modelo de gestión del servicio farmacéutico (Resolución 1403 de 2007) respecto del embalaje, transporte y entrega física de medicamentos, dispositivos médicos y otros insumos relacionados.
Los laboratorios farmacéuticos continuarán regidos por las normas especiales vigentes, de conformidad con el parágrafo del artículo 2º del decreto 2200 de 2005. Cuando las Farmacias-Droguerías, Droguerías o las personas autorizadas, sean contratadas para la prestación de servicios dentro del Sistema General de Seguridad Social en Salud, deberán cumplir íntegramente con lo establecido en el decreto 2200 de 2005 y la Resolución 1403 de 2007 el (modelo de gestión del servicio farmacéutico).
Las Farmacias-Droguerías, Droguerías, Agencias de Especialidades Farmacéuticas, Depósitos de Drogas y personas autorizadas, teniendo en cuenta el volumen de actividades y el número de trabajadores que laboren en estos, deberán tener una estructura acorde con los procesos que realicen; ubicación independiente; área física exclusiva, de circulación restringida y de fácil acceso; iluminación, ventilación, pisos, paredes, cielos rasos, instalaciones sanitarias y eléctricas, que permitan la conservación de la calidad de los medicamentos, dispositivos médicos y demás productos autorizados, así como, someterse a las demás condiciones que se establezcan en la Resolución 1403 de 2007.
En las agrupaciones de droguerías de un mismo propietario, cada cinco (5) de ellas estarán bajo la dirección de un Químico Farmacéutico, sin perjuicio de que en cada uno de estos sitios esté a cargo del Expendedor de Drogas o el recurso humano autorizado para estos establecimientos.
Los establecimientos farmacéuticos que se encarguen de realizar una o más actividades y/o procesos propios del servicio farmacéutico por cuenta de otra persona, deberán cumplir para ello con las condiciones y requisitos establecidos por el decreto 2200 de 2005, la Resolución 1403 de 2007 (modelo de gestión del servicio farmacéutico) y demás normas que regulen las respectivas actividades y/o procesos, responsabilizándose solidariamente con la contratante ante el Estado y los usuarios, beneficiarios o destinatarios por los resultados de la gestión.

Cuando en estos establecimientos farmacéuticos se realicen operaciones de elaboración, transformación, preparaciones, mezclas, adecuación y ajuste de concentraciones de dosis, reenvase o reempaque de medicamentos, deberán obtener el Certificado de Cumplimiento de Buenas Prácticas de Manufactura, otorgado por el Instituto Nacional de Vigilancia de Medicamentos y Alimentos, INVIMA, y su dirección técnica estará a cargo exclusivamente de Químico Farmacéutico.
Los productos allí elaborados no requieren de registro sanitario. El establecimiento farmacéutico o servicio farmacéutico institucional podrá funcionar con la autorización o habilitación por parte de la entidad territorial de salud o el Certificado de Cumplimiento de Buenas Prácticas de Manufactura otorgado por el Instituto Nacional de Vigilancia de Medicamentos y Alimentos, INVIMA, para aquellos establecimientos a los que se les exige, según corresponda.
Cuando estos establecimientos farmacéuticos realicen actividades y/o procesos propios del servicio farmacéutico a una Institución Prestadora de Servicios de Salud se someterán a la normatividad aplicable a dicha actividad y/o proceso, sin perjuicio de la responsabilidad de la Institución Prestadora de Servicios de Salud respecto al cumplimiento de los estándares de cada una de las actividades y/o procesos.

Para implementar un sistema de gestión de compras, ¿Qué se debe tener en cuenta?
Disminución del costo o mantener un costo justo, controlado y apropiado que cumpla con los requisitos que exige el producto final. Las variables de influencia crucial en la toma de decisiones de compra son los proveedores. No todo proveedor puede ser parte del sistema de producción y menos aquellos que solo juegan al papel del intermediario para obtener una comisión sin conocer las características del bien objeto de la compra. Otra variable también de gran influencia en la decisión de la compra, es el entorno del mercado y por eso es necesario conocer cadenas de abastecimiento internacionales, que superan en responsabilidad, manejo y suministro de bienes a los proveedores locales. La empresa que compra por unidades en el mercado local está sujeta a la diferencia de calidad, a las variaciones de precio y a los traumas de entrega oportuna.
Un sistema de gestión de compras es necesario para gestionar adecuadamente los suministros
Las personas que se encargan de las compras en una organización, tienen la responsabilidad de optimizar el rendimiento en la cadena de suministro.
Si antes eran funcionarios que solo se dedicaban a pedidos, la tendencia universal es contar con un profesional competente, experto en planeación, con buena experiencia en controles y seguimiento para tener la compra en el tiempo oportuno, al precio adecuado y con la calidad requerida.
De las decisiones del gestor de compras depende:
- La eficiencia de procesos.
- El control apropiado de costos.
- La alineación con la estrategia empresarial.
Su misión está integrada con el negocio en conjunto y sus acciones causan un impacto en todas las áreas, por eso su misión se desarrolla con base en la pro-actividad y exige:
- La búsqueda continua de nuevos materiales y oportunidades.
- La comparación de proveedores, ofertas y fuentes de aprovisionamiento.
- La coherencia en sus decisiones y la capacidad de hacer pronósticos con base en datos objetivos y fiables.
- El velar por dar el mejor uso a los recursos monetarios de la empresa llevando a cabo una impecable gestión de stock.

En un sistema de gestión de compras se debe tener en cuenta
Cualquier sistema que permita gestionar compras debe tener en cuenta algunos factores clave, que permiten reducir el riesgo y a la vez que incrementan la eficacia:
Las necesidades: conocer las cartas de producto de la organización, en forma concreta para diferenciar cada presentación y hacer que las necesidades de la empresa se puedan enfocar a una mejor planificación de la demanda, que se reflejará en condiciones óptimas de la función de aprovisionamiento, disfrutar de descuentos por grandes volúmenes, ofertas especiales o condiciones más beneficiosas atendiendo a la periodicidad de compra.
Los proveedores: Es conveniente crear o mantener activa una relación entre Proveedor – Entrada – Proceso – Entregas – Cliente. Con esta relación se puede controlar, calificar y determinar las características del proveedor que permita relacionar la materia prima con el cliente final. Igualmente algunas variables que permitan seleccionar el proveedor apropiado para el producto requerido. El mercado de los productos se entiende mejor, en la medida en que cada proveedor se especialice por líneas de productos que guarden relación para almacenamiento, transporte, entregas y su solidez financiera le permitan cumplir oportunamente con las entregas. Es muy importante tener en cuenta el servicio posventa para tomar la decisión de selección.
El mercado: La oferta de productos permite comparar y generar una idea de las condiciones del mercado y facilita una buena selección. Conformarse con la primer oferta, es un riesgo que no se debe asumir, tampoco es conveniente excederse en esta etapa y aumentar innecesariamente la lista de proveedores a evaluar.
Producto: Experimentar nuevos productos, evaluar proveedores alternativos, abrir concursos de compra entre distintas empresas, puede aportar una gran ventaja y evita la dependencia que sitúa al proveedor en una posición indispensable que no beneficia a la empresa.
Demanda: la curva de la demanda, el ritmo de la competencia y la tendencia del mercado plantean desafíos a los que la organización tiene que responder. La ventaja en costos es siempre un buen punto de partida y en ello un buen sistema de gestión de compras tiene mucho que decir.
En un sistema de compras se debe evitar- Pretender que las ofertas de los proveedores son iguales excepto el precio. Muchos proveedores se esfuerzan por diferenciar sus productos o servicios. Es conveniente comprender esas diferencias y descubrir qué valor tienen para la organización, que permita una buena elección.
- Aceptar condiciones imposibles de aceptar por que la empresa: Centrarse exclusivamente en el precio, pueden llevar a la tentación de hacer cualquier cosa para lograr el deseado ahorro.
- Hacer concesiones comerciales a cambio de obtener precios más bajos requiere conocer a fondo los límites, de lo contrario no es una opción a plantearse.
- Carecer de la capacidad para llegar a un consenso entre las partes interesadas para las decisiones de compra. Informar a las partes interesadas aumenta las posibilidades de éxito y disminuye posibles de conflictos.
- Desatender las propuestas de los proveedores: estas alternativas pueden ayudar a lograr lo mismo de una forma mejor o más barata. El proveedor debe tener la oportunidad de sugerir otras opciones. Fortalece las oportunidades de mejora.
- Seleccionar un proveedor sin investigar más allá de su propuesta: la selección de proveedor se debe hacerse con base en su idoneidad, valorada objetivamente, no por la capacidad de persuasión de su propuesta. Es necesario aplicar métodos de calificación y, nunca lanzarse al vacío, probar con un pequeño porcentaje de producto o durante un periodo de tiempo limitado antes de cerrar las puertas a otros.

Sistema de evaluación de proveedores
La evaluación de los proveedores es un requisito que debe tenerse en cuenta por las organizaciones que implantan ISO 9001.
Es común que la traducción de este requisito se sitúe en el mantenimiento de registros papel, llamados “Evaluación de proveedores” o algo similar, donde cada cierto tiempo se generan notas a los proveedores con base en los criterios más variados, registros que a nadie interesan (salvo al auditor), y que no se utilizan.
Es conveniente diseñar un manual de evaluación de proveedores con base en variables objetivas que guarden relación con la oportunidad, la calidad del producto, la disponibilidad, la experiencia en el manejo de imprevistos, el cuidado y almacenamiento del producto.
Estas variables deben ser calificadas por un equipo interdisciplinario que permita darle el justo valor a cada variable.
1. Evaluación inicial del Sistema de Gestión de la Seguridad y Salud en el Trabajo.
La evaluación inicial deberá realizarse una única vez, por personal idóneo de acuerdo con la normatividad vigente, incluidos los estándares mínimos, con el fin de identificar las prioridades en SST.
Se utiliza para establecer el plan de trabajo anual o para la actualización del existente.
Para cumplir con lo anterior, cada empresa puede crear un formato. Sin embargo en cualquier caso, la evaluación debe contener como mínimo los siguientes aspectos y los estipulados en los estándares mínimos:
a) La identificación de la normatividad vigente en materia de riesgos laborales incluyendo los estándares mínimos del Sistema de Garantía de Calidad del Sistema General de Riesgos laborales para empleadores, que se reglamenten y le sean aplicables.b) La verificación de la identificación de los peligros, evaluación y valoración de los riesgos, la que debe ser anual. En la identificación de peligros deberá contemplar los cambios de procesos, instalaciones, equipos, maquinarias, entre otros.
c) La identificación de las amenazas y evaluación de la vulnerabilidad de la empresa debe ser anual. d) La evaluación de la efectividad de las medidas implementadas, para controlar los peligros, riesgos y amenazas, que incluya los reportes de los trabajadores debe ser anual.
e) El cumplimiento del programa de capacitación anual, establecido por la empresa, incluyendo la inducción y re-inducción para los trabajadores dependientes, cooperados, en misión y contratistas.
f) La evaluación de los puestos de trabajo en el marco de los programas de vigilancia epidemiológica de la salud de los trabajadores.
g) La descripción sociodemográfica de los trabajadores y la caracterización de sus condiciones de salud, así como la evaluación y análisis de las estadísticas sobre la enfermedad y la accidentalidad y registro y seguimiento a los resultados de los indicadores definidos en el SG-SST de la empresa del año inmediatamente anterior.
h) Registro y seguimiento de los resultados de los indicadores definidos en el SG SST de la empresa del año inmediatamente anterior.
2. Identificación de peligros evaluación y valoración de los riesgos
La identificación de peligros, evaluación y valoración de los riesgos debe ser desarrollada por el empleador con la participación y compromiso de todos los niveles de la empresa.
Debe ser documentada y actualizada de acuerdo a lo siguiente:
- Anualmente.
- Cada vez que ocurra un accidente de trabajo mortal o un evento catastrófico en la empresa.
- Cuando se presenten cambios en los procesos, en las instalaciones en la maquinaria o en los equipos.
El empleador debe adoptar una metodología para la identificación, evaluación, valoración y control de los peligros y riesgos de la empresa. Dicha metodología debe contemplar los siguientes aspectos:
- Todos los procesos.
- Actividades rutinarias y no rutinarias.
- Actividades internas o externas.
- Maquinaria y equipos de trabajo.
- Todos los centros de trabajo.
- Todos los trabajadores, independiente de su forma de contratación o vinculación con la organización.
- Medidas de prevención y control (Jerarquización). Con el fin de proporcionar un marco de referencia, a continuación se relacionan algunas metodologías:
- Guía Técnica Colombiana GTC 45 Guía para la identificación de los peligros y la valoración de los riesgos en seguridad y salud ocupacional.
- Evaluación general del riesgo, según el Instituto Nacional de Seguridad e Higiene del Trabajo, de España.
- HAZOP
- AMFE
- AMFEC
- UCSIP
- MOSAR
- DELPHI
- UNE EN-1050-1997
Una vez identificados los peligros, evaluados y valorados los riesgos cada empresa puede identificar las medidas de prevención y control necesarias de acuerdo con la valoración obtenida. En los anexos que se relacionan a continuación, se establece metodología propuesta por el Ministerio del Trabajo, para la MIPYME empresa (Que no tenga actividades de alto riesgo) con su respectivo formato.
3. Política y Objetivos de Seguridad y Salud en el Trabajo
Política de Seguridad y Salud en el Trabajo
El empleador o contratante establecerá, por escrito, una política de Seguridad y Salud en el Trabajo -SST la que debe ser parte de las políticas de gestión de la empresa. Debe cubrir todos los centros de trabajo y a todos los trabajadores, independiente de su forma de, contratación o vinculación, incluyendo los contratistas y subcontratistas.
Importancia de elaborar una política
Es fundamental antes de cualquier planificación preventiva definir la política empresarial en materia de prevención de riesgos laborales.
La debe la Dirección y contará con el apoyo de los trabajadores o de sus representantes. Corresponderá a una declaración de principios y compromisos que promuevan el respeto a las personas y a la dignidad de su trabajo, la mejora continua de las condiciones de seguridad y salud dentro de la empresa.
4. Plan de Trabajo Anual del Sistema de Gestión de la Seguridad y Salud en el Trabajo y asignación de recursos
Se requiere diseñar y desarrollar un Plan de trabajo anual del SG-SST, contemplará información de entrada, como por ejemplo:
- Evaluación inicial.
- Identificación de Peligros, evaluación y valoración de riesgos.
- Resultados de las auditorías internas.
- Revisiones por la alta dirección.
- Acciones preventivas y correctivas.
En el Plan de trabajo anual del SG-SST de cada empresa se debe identificar como mínimo lo siguiente:
- Metas.
- Responsabilidades.
- Recursos (financieros, técnicos y el personal necesario).
- Cronograma de actividades.
5. Capacitación, Entrenamiento, Inducción y Re-inducción en SST.
Se definirán los temas mínimos, especialmente cuando se traten temas asociados a las actividades críticas de la organización, teniendo en cuenta los resultados obtenidos de la aplicación de la metodología de identificación de peligros, evaluación y valoración de los riesgos.
En el Programa de capacitación, entrenamiento, inducción y re-inducción en SST, se deben tener en cuenta los aspectos relacionados con la prevención y promoción de la seguridad y salud de los trabajadores y puede incluir:
- Identificación de las necesidades de capacitación y/o entrenamiento en el SG-SST, por nivel y su actualización de acuerdo con las necesidades de la empresa.
- Temas mínimos por grupos de interés (brigada, vigía o COPASST, alta dirección, trabajadores).
- Objetivo.
- Alcance.
- Contenido.
- Registros de las personal a capacitar.
Para determinar las necesidades del Programa de Capacitación se debe tener en cuenta las competencias requeridas por los trabajadores para el desempeño seguro de su labor:
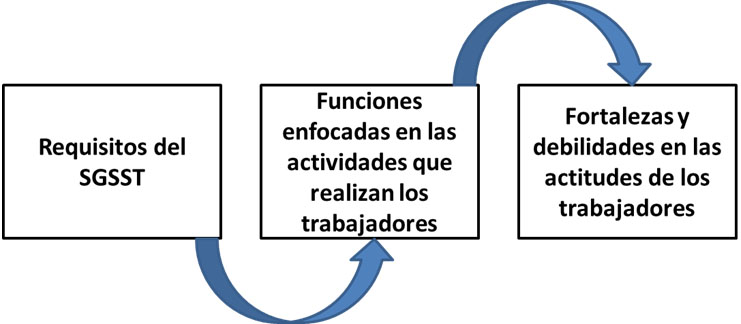
El empleador debe proporcionar a todo trabajador que ingrese por primera vez a la empresa, independiente de su forma de contratación, vinculación y de manera previa al inicio de sus labores, una inducción en los aspectos generales y específicos de las actividades a realizar, que incluya entre otros, la identificación y el control de peligros y riesgos en su trabajo y la prevención de accidentes de trabajo y enfermedades laborales. Así mismo se realizará re-inducción a todos los trabajadores, independiente de su forma de contratación y vinculación.
6.- Prevención, preparación y respuesta ante emergencias.
Es obligatorio implementar y mantener las disposiciones necesarias en materia de prevención, preparación y respuesta ante emergencias, con cobertura a todos los centros, turnos de trabajo y todos los trabajadores, independiente de su forma de contratación o vinculación, incluidos contratistas y subcontratistas, así como proveedores y visitantes.
Como complemento, se debe mantener actualizada la identificación sistemática de amenazas y el análisis de la vulnerabilidad de las mismas que puedan afectar a la empresa; igualmente se debe contar con las medidas de protección acordes con las amenazas detectadas, éstas responderán eficaz y efectivamente a una emergencia para reducir la afectación al entorno, ambiente, personas y a la propiedad.
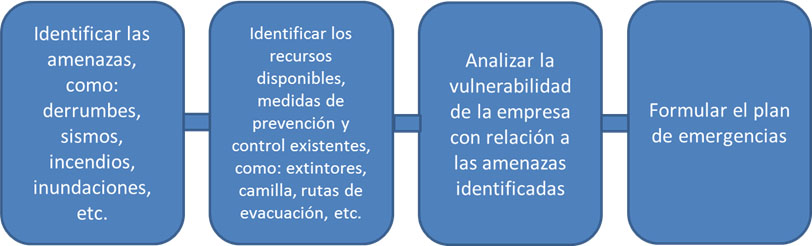
Es conveniente articularse con las instituciones locales o regionales, tales como Bomberos de Colombia, Fondo Nacional de Gestión del Riesgo de Desastres, Defensa Civil, Cruz Roja Colombiana, entre otros. Para implementar un Plan de prevención, preparación y respuesta ante emergencias considere lo siguiente:
7.- Reporte e investigación de incidentes, accidentes de trabajo y enfermedades laborales.
Las empresas deben reportar e investigar todos los accidentes de trabajo y enfermedades laborales calificadas, además de investigar los reportes de incidentes.
El empleador o contratante está obligado a reportar a la ARL y EPS TODOS los accidentes de trabajo y enfermedades laborales diagnosticadas de los trabajadores, incluyendo los vinculados a través de contrato de prestación de servicios dentro de los dos (2) días hábiles siguientes a la ocurrencia del accidente o al diagnóstico de la enfermedad laboral. Copia del este reporte deberá suministrarse al trabajador.
SOLO los accidentes graves y mortales, como las enfermedades laborales diagnosticadas deberán ser reportados a la Dirección Territorial u Oficina especial del Ministerio del Trabajo dentro del término ya mencionado.
Cuando se presente un accidente de trabajo
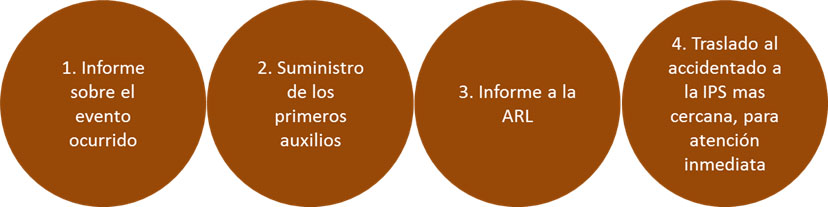
El reporte de accidente de trabajo o enfermedad laboral lo diligenciará el empleador o contratante, o sus delegados o representantes.
Es necesario demostrar la existencia del registro y reporte de los accidentes e incidentes y enfermedades diagnosticadas.
El no reporte puede acarrear una multa de hasta 1.000 s.m.m.l.v. y el reporte extemporáneo hasta 500 s.m.m.l.v.
Investigación de incidentes y accidentes de trabajo
El empleador o contratante debe investigar TODOS los accidentes e incidentes de los trabajadores, incluyendo los vinculados a través de contrato de prestación de servicio, dentro de los quince (15) días siguientes a su ocurrencia (calendario). SOLO en caso de accidente grave o mortal se deberá remitir la investigación a la Administradora de Riesgos Laborales, dentro del término ya mencionado.
Esta investigación debe realizarse a través del equipo investigador, el que debe estar conformado como mínimo por:
- El jefe inmediato o supervisor del trabajador accidentado o del área donde ocurrió el incidente
- Un representante del Comité Paritario o el Vigía de Seguridad y Salud en el Trabajo.
- El responsable del desarrollo del Sistema de Gestión de la Seguridad y Salud en el Trabajo.
- Cuando el accidente se considere grave o produzca la muerte, en la investigación deberá participar un profesional con licencia en Seguridad y Salud en el Trabajo, propio o contratado.
Aspectos a tener en cuenta en las investigaciones de incidentes o accidentes de trabajo:
- Establecer un mecanismo para realizar la investigación de los accidentes e incidentes que incluya todos los parámetros definidos en la Resolución 1401 de 2007 o que la modifique o complemente.
- Establecer acciones preventivas, correctivas y de mejora necesarias.
Es importante determinar las causas del evento, para ello puede utilizar alguna de las siguientes metodologías:
- Diagrama causa-efecto.
- Teoría de los cinco porqués.
- Lluvia de ideas.
- Benchmarking (Medida de Calidad).
- Taproot
- Tasc – Técnica de Análisis Sistemático de Causas
El resultado de la investigación debe permitir, entre otros, lo siguiente:
- Identificar y documentar las deficiencias del SGSST.
- Informar los resultados a los trabajadores directamente relacionados con sus causas o controles.
- Informar a la alta dirección sobre el ausentismo laboral por incidentes, accidentes y enfermedades laborales.
- Alimentar la revisión de la alta dirección.

8. Criterios para adquisición de bienes o contratación de servicios con las disposiciones del SG-SST.
Adquisición de bienes
La empresa debe establecer y mantener un procedimiento para adquisiciones, con el fin de garantizar que se identifiquen y evalúen en las especificaciones relativas a las compras o adquisiciones de productos y servicios, las disposiciones relacionadas con el cumplimiento del Sistema de Gestión de la Seguridad y Salud en el Trabajo SG-SST por parte de la empresa.
Contratación
El empleador debe considerar como mínimo los siguientes aspectos para sus proveedores, trabajadores dependientes, trabajadores cooperados, trabajadores en misión, contratistas y sus trabajadores o sub contratistas durante el desempeño de las actividades objeto del contrato:
- Aspectos de seguridad y salud en el trabajo para la selección y evaluación.
- Procurar canales de comunicación para la SST.
- Verificar antes del inicio del trabajo y periódicamente la afiliación al Sistema General de Riesgos Laborales.
- Informar previo al inicio del contrato los peligros y riesgos generales y específicos de su zona de trabajo.
- Informar sobre los presuntos accidentes de trabajo y enfermedades laborales ocurridas.
- Verificar periódicamente y durante el desarrollo de las actividades objeto del contrato, el cumplimiento de la normatividad en SST.
9. Medición y evaluación de la gestión en SST.
Indicadores de estructura, proceso y resultado que miden el SG-SST.
Por medio de los indicadores se verifica el cumplimiento del SG-SST y de acuerdo con los resultados se establecen las acciones correctivas, preventivas o de mejora necesarias.
El empleador debe definir los indicadores (cualitativos o cuantitativos según corresponda) mediante ellos se evaluarán la estructura, el proceso y los resultados del SG-SST y debe hacer seguimiento a los mismos. Estos indicadores deben alinearse con el plan estratégico de la empresa y hacer parte del mismo.
Se debe realizar una ficha técnica para cada indicador, en la que se pueden tener en cuenta las siguientes variables:
| PARÁMETRO | EJEMPLO |
|---|---|
| 1. Definición del indicador | Cumplimiento del plan de trabajo anual |
| 2. Interpretación del indicador | Es un indicador de proceso que evalúa el cumplimiento de las actividades planificadas. |
| 3. Límite del indicador o valor a partir del que se considera que cumple o no con el resultado esperado | Cumple ≥ al 90% En riesgo ≥ 80% y < 90% Crítico < 80% |
| 4. Método de cálculo | (Número de actividades ejecutadas / Número de actividades programadas del plan de trabajo anual) * 100 |
| 5. Fuente de información para el cálculo | Plan anual de trabajo y soportes |
| 6. Periodicidad del reporte (Cada cuanto se va a analizar) | Trimestral |
| 7. Personas que deben conocer el resultado | Empleador y Responsable del SG-SST. |
Los indicadores del SG-SST se dividen en tres tipos:
Indicadores que evalúan la estructura del SG-SST:
Medidas verificables de la disponibilidad y acceso a recursos, políticas y organización con que cuenta la empresa para atender las demandas y necesidades en Seguridad y Salud en el Trabajo, ejemplo:
• Número de requisitos del numeral 2.2.4.6.20 que cumplan con las especificaciones del Decreto 1072 / número de requisitos solicitados por dicho numeral
Indicadores que evalúan el proceso del SG-SST:
Medidas verificables del grado de desarrollo e implementación del SG-SST, ejemplo:
• Número de actividades cumplidas del plan anual de trabajo / número de actividades programas en el plan anual de trabajo.
Indicadores que evalúan el resultado del SG-SST:
Medidas verificables los cambios alcanzados en el periodo definido, teniendo como base la programación y la aplicación de recursos propios del programa o del sistema de gestión, ejemplo:
• Número de accidentes ocurridos en el periodo
• Número de accidentes del periodo anterior / accidentes del periodo anterior.
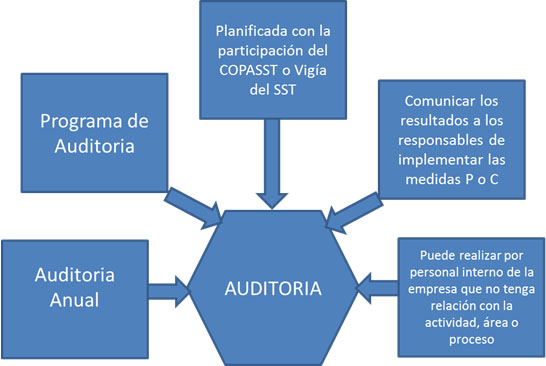
El programa de auditoría interna debe comprender como mínimo, lo siguiente:
- Definir la idoneidad del (de los) auditor (es) internos.
- El alcance de la auditoría.
- La periodicidad de la auditoría.
- La metodología y la presentación de los informes.
El alcance de la auditoria interna debe abarcar entre otros lo siguiente:
- El cumplimiento de la política de seguridad y salud en el trabajo.
- El resultado de los indicadores de estructura, proceso y resultado.
- La participación de los trabajadores.
- El desarrollo de la responsabilidad y la obligación de rendir cuentas.
- El mecanismo de comunicación de los contenidos del SG – SST a los trabajadores.
- La planificación, desarrollo y aplicación del SGSST.
- La gestión del cambio.
- La consideración de la seguridad y salud en el trabajo en las nuevas adquisiciones.
- El alcance y aplicación del SG SST frente a los proveedores y contratistas.
- La supervisión y medición de los resultados.
- El proceso de investigación de incidentes, accidentes de trabajo y enfermedades laborales, y su efecto sobre el mejoramiento de la seguridad y salud en el trabajo en la empresa.
- El desarrollo del proceso de auditoría.
- La evaluación por parte de la alta dirección.

Revisión anual al SG-SST por parte de la alta dirección.
La revisión por la alta dirección es un informe ejecutivo en el que se verifica el grado de cumplimiento del SG -SST, esta se debe hacer por lo menos una vez al año.
La revisión de la alta dirección debe permitir revisar lo establecido en el Artículo 2.2.4.6.31 del Decreto 1072 de 2015.
La información de entrada para la revisión por la alta dirección debe incluir:
- Estrategias implementadas en SST.
- Plan de trabajo anual.
- Recursos asignados al SG-SST.
- Satisfacción de necesidades de SST.
- Cambios del SG-SST.
- Revisiones por la alta dirección, anteriores.
- Resultado de indicadores del SG-SST.
- Resultado de auditorías del SG-SST.
- Prioridades en SST detectadas.
- Política y objetivos de SST.
- Eficacia de las medidas de prevención y control.
- Rendición de cuentas sobre el desempeño de los trabajadores en SST.
- Identificación de peligros, evaluación y valoración de los riesgos.
- Gestión de peligros.
- Promoción de la participación de los trabajadores en la SST.
- Cumplimiento de normatividad.
- Acciones correctivas, preventivas o de mejora.
- Inspecciones de trabajo en SST.
- Vigilancia de las condiciones de salud de los trabajadores.
- Reporte e investigación de los incidentes, accidentes de trabajo y enfermedades laborales.
- Ausentismo laboral.
- Programas de rehabilitación de la salud de los trabajadores.
La revisión por la alta dirección debe estar documentada y los resultados de la misma deben ser divulgados al COPASST o Vigía de Seguridad y Salud en el Trabajo y al responsable del Sistema de Gestión de la Seguridad y Salud en el Trabajo SG-SST quienes deberán definir e implementar las acciones preventivas, correctivas y de mejora a que hubiese lugar.
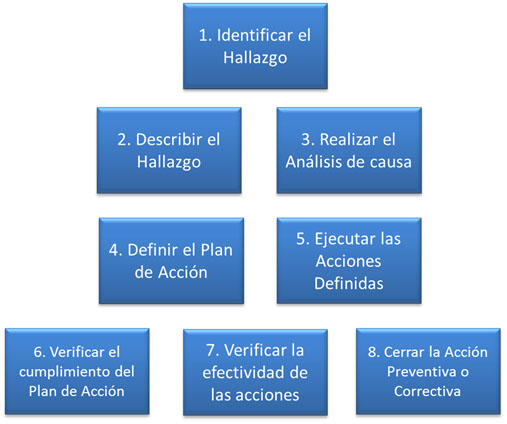
10. Acciones preventivas o correctivas
El empleador debe definir e implementar acciones correctivas o preventivas, esto con el fin de gestionar las no conformidades reales o potenciales que puedan influir en una desviación del SG-SST.
Las acciones pueden ser derivadas, entre otras, de las siguientes actividades:
- Resultados de las inspecciones y observación de tareas.
- Investigación de incidentes y accidentes de trabajo.
- Auditorías internas y externas.
- Sugerencias de los trabajadores.
- Revisión por la Alta Dirección.
- Cambios en procedimientos o métodos de trabajo.
Lo anterior debe contemplar una metodología que permita eliminar la causa raíz.
La organización debe asegurarse de documentar y soportar el plan de acción definido en la acción correctiva o preventiva y verificar si estas fueron efectivas.
Para determinar el plan de acción, se puede seguir el siguiente esquema: